Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Détourner le métabolisme des tumeurs pour mieux les détruire…
- Tweeter
-
-
0 avis :
Les travaux du Professeur Olivier Feron, chercheur à l’Institut de recherche expérimentale et clinique de l’UCL, et son équipe, ont pour objectif d’inhiber les mécanismes métaboliques qui permettent aux tumeurs de grandir. Ces chercheurs avaient déjà montré qu'à côté du glucose, les cellules cancéreuses pouvaient trouver de l’énergie en recyclant certains déchets métaboliques qui seraient produits soit ailleurs dans la tumeur, soit dans des organes sains puis véhiculés par le sang jusque dans la tumeur. Mais cette équipe de recherche est cette fois allée plus loin et a découvert ce qui, dans une tumeur, détermine l'utilisation, soit du glucose, soit du lactate.
Ces chercheurs ont en effet montré qu' une protéine appelée MPC (mitochondrial pyruvate carrier), localisée dans la membrane des mitochondries, transporte le pyruvate dans la mitochondrie et constitue le dénominateur commun à l'oxydation du glucose et du lactate dans la cellule. Les mitochondries sont quant à elles des usines intracellulaires capables - entre autres - d'extraire l'énergie du pyruvate et de produire la matière première nécessaire à la croissance des cellules cancéreuses.
Mais ces scientifiques ont également identifié une molécule - 7ACC2- qui est non seulement capable d’empêcher le lactate d’être exploité comme substrat énergétique, en bloquant l'utilisation du glucose et du lactate par les mitochondries des cellules cancéreuses, mais empêche de surcroit l'oxygène d'être consommé par la tumeur pour augmenter indirectement sa disponibilité. On obtient alors une augmentation très sensible de l'efficacité de la radiothérapie. Le Professeur Feron précise que cette molécule 7ACC2 devrait être expérimentée sur l'homme en 2020.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :
Cancer du sein : l’Institut Curie veut bloquer la maladie dès ses origines
Dans les laboratoires de l’Institut Curie, les chercheurs décortiquent les mécanismes biologiques, génétiques et épigénétiques qui entrent en jeu au moment où la tumeur se forme puis se développe. ...

Une molécule dans les légumes crucifères pourrait protéger des infections pulmonaires
Dans une étude récente, des chercheurs du Francis Crick Institute de Londres ont découvert que les molécules naturellement présentes dans les légumes crucifères, comme le brocoli et le chou-fleur, ...
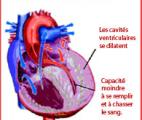
Découverte d’un nouveau mécanisme moléculaire de l’insuffisance cardiaque
Dans l’insuffisance cardiaque, le cœur ne parvient plus à alimenter correctement l’organisme en sang, ce qui affecte durement la qualité de la vie. La protéine EPAC1 est une cible thérapeutique de ...
Recommander cet article :
- Nombre de consultations : 301
- Publié dans : Biologie & Biochimie
- Partager :